|
Bohrsches Postulat, Materiewellen, Unschärferelation: Alles hing irgendwie
zusammen, beantwortete bisher ungelöste Fragen, gab sogar - durch das Experiment überprüft - quantitativ
richtige Antworten auf einige Fragen - aber letztlich war das alles nur Stückwerk, es fehlte der große theoretische
Überbau. |
 |
1925 erschien das "Dreimännerwerk": Werner Heisenberg, Max Born
und Pascal Jordan "erfanden" (oder "fanden"?) und veröffentlichten eine konsistente mathematische Theorie
der Welt der Atome, die Quantenmechanik. |
|
 |
Ihr mathematisches Gerüst beruhte auf der (den Physikern damals fremdartigen) Matrixalgebra. |
|
 |
Wolfgang Pauli
zeigte dann, daß die Bohrsche Version des Wasserstoffatom ganz organisch (wenn auch mit beträchtlichem mathematischem
Aufwand) in der neuen Quantemechanik steckte. Der Durchbruch war erreicht. Doch die algebraische Quantenmechanik war schwer
und unanschaulich. |
 |
Aber gleich darauf, 1926, brachte Erwin Schrödinger die Quantentheorie
in die gebräuchlichste Form, ausgedrückt in einer (den Physikern geläufigen) partiellen Differentialgleichung
vom Typus einer Wellengleichung, eben der berühmten Schrödingergleichung . |
|
 |
Kurz danach konnte er auch zeigen - was durchaus nicht offensichtlich ist - daß
die Heisenbergsche Matrizen-Quantenmechanik und seine Wellengleichung exakt dasselbe beschrieben, lediglich in anderer (mathematischer)
Sprache. |
 |
Lösungen der Schrödingergleichung führten zu exakt
denselben Energien der Elektronen des Wasserstoffatoms, die schon Bohr erhielt - aber die Schrödingergleichung war
ein neues Axiom, ein neues universelles Naturgesetz, und nicht nur eine Erweiterung
der klassischen Mechanik mit künstlichen Quantenbedingungen. |
|
 |
Sie war universell anwendbar und nicht auf das Wasserstoffatom
beschränkt. |
|
 |
Die Schrödingergleichung verleiht allen
Teilchen (auch großen) Welleneigenschaften. Das Problem des Wasserstoffatoms reduziert sich auf das Auffinden
der Lösungen, die für das gegebene Potential die möglichen (dreidimensionalen) stehenden
Wellen beschreiben. Mathematisch ist das nahezu identisch mit der Berechnung stehender akkustischer Wellen in einem kugelförmigen
Resonator - schwierig, aber nichts besonderes. |
|
 |
Stehende Wellen müssen es sein, denn "laufende" Wellen würden ja bedeuten,
daß das Atom auseinanderfließt. |
 |
Das große Problem war und ist aber: Was exakt "wellt"? In der
Schrödingergleichung ist es einfach ein neuer mathematischer Begriff, die Wellenfunktion
y(r)
des Teilchens (oder, bei mehreren Teilchen mit den Ortsvektoren r1, r2,
...ri dann die Wellenfunktion y(r1,
r2, ...r i) des Systems). |
|
 |
Strikt mathematisch gesehen, ist y(r
) irgendeine Funktion. Physikalisch gesehen muß y( r
) aber "irgendwie" das physikalische System beschreiben, für das wir die Schrödingergleichung
aufgestellt und gelöst haben. Und eine physikalische Beschreibung heißt immer, daß wir ausrechnen
können, was wir in einem Experiment messen werden. |
|
 |
In y(r) müssen also messbare Dinge -
Ort, Impuls, Energie, usw. - codiert sein, wenn es physikalisch signifikant sein soll. |
 |
Widmen wir uns also den Eigenschaften der Wellenfunktion y(r).
Ein erster Stolperstein beim Versuch zu verstehen was y(r) darstellt ist
die Tatsache, daß y(r) in der Regel eine komplexe
Größe ist - das gab es in der Physik bisher nicht! |
|
 |
Aufpassen! Die Tatsache, daß man
auch in der klassischen Physik mit Hilfe der Eulerbeziehung
gelegentlich komplex rechnet um mathematisch eleganter vorgehen zu können, bedeutet
nicht, daß die behandelten Größen selbst komplex sind. Im Zweifel ist
immer nur der Realteil gemeint! Dies gilt insbesondere bei der Behandlung des Wechselstroms
in der Elektrotechnik, aber auch z.B. bei der Behandlung von klassischer Interferenz. |
 |
Mit einer intrinsisch oder inherent komplexen Wellenfunktion als Beschreibung
einer physikalischen Realität erfolgt also ein kompletter Bruch sowohl mit der klassischen Physik,
als auch mit der herkömmlichen Betrachtung der Natur, der Naturphilosophie oder Metaphysik. |
|
 |
Da wir keine imaginären messbaren Größen kennen, folgt sofort, daß die
Wellenfunktion eine höhere Abstraktionsebene darstellt als die gewohnten meßbaren physikalischen Größen.
Sie kann also nicht direkt gemessen werden, sondern muß die gewünschte Information "codiert" enthalten. |
|
 |
Die Schrödingergleichung ist damit erstmals in
der Physik eine Gleichung für eine abstrakte
Größe, eine Größe die nicht mehr direkt gemessen werden kann, und die damit den menschlichen
Sinnen unzugänglich bleibt. Denn nur was sich über ein (noch so kompliziertes) Meßgerät in eine Größe
transformiert, die der Mensch sehen, hören, fühlen, schmecken oder riechen kann, betrachten
wir als real, als unmittelbar existent. |
|
 |
Die Diskussion über die "wirkliche" Bedeutung der Wellenfunktion hält
an. Gerade jetzt lebt sie wieder auf; ein Blick auf die in den letzten Jahren veröffentlichten populärwissenschaftlichen
Bücher zum Thema - meistens von Physik Nobelpreisträgern - zeigt dies ganz plastisch. |
 |
Obwohl es ungeheuer reizvoll sein kann, sich mit dieser Thematik zu beschäftigen
- es handelt sich letzlich um eine der wenigen ganz großen intellektuellen Herausforderungen, die sich der Wissenschaft
noch stellen (eine andere Herausforderung dieser Größenordnung ist z.B. die Frage nach der "Natur"
des Bewußtseins (Was ist Leben, insbesondere bewußtes Leben?))
- müssen wir uns im Rahmen der Einführung in die Materialwissenschaft darum nicht kümmern. Wir nehmen einfach
nur folgenden Satz zur Kenntnis: |
|
|
Das Betragsquadrat
|y(r)|2
der Wellenfunktion y(r)
eines Teilchens
an einem gegebenen Ort r = (x,y,z)
ist ein Maß für die Wahrscheinlichkeit,
daß das betrachtete Teilchen an diesem Ort zu finden ist. |
|
 |
Diese Aussage, die wir hier einfach als eine Art Axiom hinnehmen, gilt es nun
mathematisch auszudrücken: |
|
|
|
|
 |
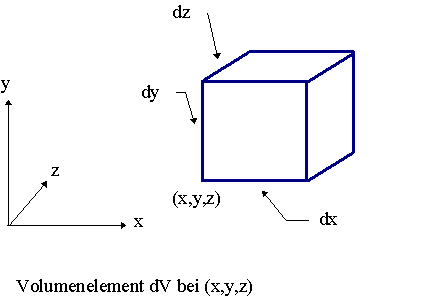
Den Ort definieren als ein differentielles Volumenelement dV
; also als ein Würfelchen mit einer Ecke bei der betrachteten Koordinate (x,y,z) und der Kantenlänge
dx, dy, dz. |
|
 |
Am Ort (x,y,z) hat die Wellenfunktion den (komplexen) Wert y(x,y,z). |
| |
Das Betragsquadrat der Wellenfunktion ist gegeben durch
|
| |
| Betragsquadrat | = |
y(x,y,z ) · y*(x,y,z) |
|
|
|
 |
d.h. der komplexe Wert der Funktion an der Stelle (x,y,z) multipliziert mit
dem konjugiert komplexen Wert y*(x,y,z) . Es
ist damit schlicht der Betrag der komplexen
Zahl, machmal auch Modul genannt. |
|
 |
Die Wahrscheinlichkeit w(x,y,z), das Teilchen im betrachteten Volumenelement
dV = dxdydz zu finden, ist dann proportional zur Größe des Volumenelements
und es gilt |
|
|
| w(x,yz) | = |
y(x,y,z) · y*(x,y,z) · dxdydz |
| | |
|
w(x,yz)
dV |
= |
y (x,y,z) · y*(x,y,z) |
|
|
 |
Dies bedeutet, daß das Betragsquadrat der Wellenfunktion eine "Wahrscheinlichkeits
dichte" dafür ist, das betrachtete Teilchen bei der gewählten Koordinate zu finden.
|
|
 |
Man nennt w(x,y,z) auch die Aufenthaltswahrscheinlichkeit
des Teilchens am Ort (x,y,z); d.h. man läßt das "....dichte
" weg, da jeder und jede weiß was gemeint ist und "Aufenthaltswahrscheinlichkeitsdichte" ja auch
nicht unbedingt zu den schönsten deutschen Wörtern zählen würde. |
 |
Da die Wahrscheinlichkeit w, das Teilchen
irgendwo in einem beliebig großen Volumen
zu finden immer w = 1 sein muß, gilt grundsätzlich eine Normierungsbedingung
der Form |
| |
+¥
ó
õ
– ¥ |
+¥
ó
õ
–¥ |
+¥
ó
õ
–¥ |
y(x,y,z) · y *(x,y,z) ·
dxdydz = 1 |
|
|
 |
Die Schrödingergleichung bestimmt nun
die Wellenfunktion
y für das betrachtete System. In ihrer allgemeinsten Form ist sie eine lineare
partielle Differentialgleichung 2. Ordnung für die Variablen Ort
und Zeit der Wellenfunktion y(x,y,z,t). Wir
werden sie im 2. Teil, der Einführung in die
Materialwissenschaft II, in dieser allgemeinsten
Form der zeitabhängigen Schrödingergleichung
kennenlernen. |
|
 |
Wenn man die Differentialgleichung löst, erhält man die Wellenfunktion
für das betrachtete Problem und weiß damit, mit welcher Wahrscheinlichkeit sich die betrachteten Teilchen wo
befinden werden. |
 |
Die Wellenfunktion ist aber noch mehr. Sie enthält nämlich alle
Informationen über das betrachtete Teilchen oder System. Man kann diese Informationen über spezielle mathematische
Manipulationen der Wellenfunktion erhalten; das ist für uns an dieser Stelle aber nicht wichtig. Wer aber aus Neugier
gern mehr wissen will, soll Kapitel 16 (der 18. Auflage) im "
Gerthsen" lesen. |
|
 |
Hier wollen wir uns die Aufgabe erleichtern, und nur Systeme betrachten, in denen sich zeitlich
nichts mehr ändert - die in sich ruhend zeitlich stationär sind. Ein Beispiel
dafür ist jedes beliebige Atom, das heute so vorliegt wie gestern und morgen und in alle Zukunft - sofern von außen
nicht eingegriffen wird. |
|
 |
Für diese stationären Zustände gibt es die vereinfachte,
nämlich zeitunabhängige Schrödingergleichung
, in der die Zeit als Variable nicht mehr vorkommt. |
|
 |
Die zeitunabhängige Schrödingergleichung für ein
Teilchen der Masse m lautet |
|
|
| – |
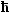 2 2
2m |
æ
ç
è |
¶2y(x,y,z)
¶x2 | + |
¶2 y(x,y,z)
¶y 2 | + |
¶2y (x,y,z)
¶ z2 |
ö
÷
ø | + |
æ
è |
U(x,y,z) – E | ö
ø
| · y(x,y,z ) = 0 |
|
|
|
 |
Dabei ist E die Gesamtenergie
, i.d.R. also kinetische plus potentielle Energie, und U die potentielle Energie des betrachteten Systems;
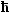 = "h quer" = h/2p hatten wir schon. = "h quer" = h/2p hatten wir schon. |
|
 |
Da der Energieerhaltungssatz
auch in der Quantenmechanik gilt, ist die Gesamtenergie
E eine feste Zahl, die nicht von den Koordinaten abhängt, während die potentielle Energie U(x,y,z)
natürlich eine beliebige Funktion der Koordinaten sein kann. |
 |
Diese vergleichsweise simple Differentialgleichung hat ungeahnte Konsequenzen.
Denn sie enthält in ihrer vollen (zeitabhängigen) Form letztlich die Newtonschen Grundgleichungen, und, in einer
erweiterten Form (dann Dirac -Gleichung genannt), die Maxwell-Gleichungen
inklusive der speziellen Relativitätstheorie ! |
|
 |
In anderen Worten: Sie ist eine der fundamentalsten Gleichungen der Physik.
|
|
 |
Mit der Schrödingergleichung wurde die gesamte Chemie ein Untergebiet der Physik - wenigstens vom
Prinzip her, wenn schon nicht in der Praxis, denn sie enthält alles was man über Atome, Moleküle und ihre
Reaktionen wissen kann - im Prinzip. |
|
 |
Wer der Schrödingergleichung hier das erste Mal begegnet,
sollte den Link betätigen. |
 |
Das einzige was wir hineinstecken, ist die potentielle Energie des Teilchens, U(x,y,z). |
|
 |
Der Energieerhaltungssatz, der
nach wie vor gültig ist, sagt uns, daß die Gesamtenergie E konstant
sein muß! Wir kennen sie nur nicht - und das bedeutet, daß sie neben der Wellenfunktion y(x,y,z)
aus der Lösung der Schrödingergleichung herauskommen muß. |
|
 |
Wie das Ganze "funktioniert", macht man sich am besten an einem Beispiel klar: |
 |
Wir stellen jetzt mal die Schrödingergleichung für das Wasserstoffatom
auf, oder, um ganz exakt zu sein, die Schrödingergleichung für das Elektron des Wasserstoffatoms. |
|
 |
Dabei muß nur für die potentielle Energie
U(r) des Elektrons im elektrischen Feld des Atomkerns (der eine pos. Elementarladung trägt),
also für das Potential des Elektrons, der richtige Ausdruck eingesetzt
werden. Er lautet |
| |
|
|
 |
wobei r den Abstand vom Atomkern bezeichnet, d.h. |
| |
| r = |r | | = |
æ
è |
x2 + y2 + z2 |
ö
ø | 1/2 |
|
|
 |
Die Schrödingergleichung lautet dann: |
| |
| – |
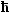 2 2
2m |
æ
ç
è |
¶2y(x,y,z )
¶x2 | + |
¶2y (x,y,z)
¶y2 | + |
¶2y(x,y,z)
¶z2 |
ö
÷
ø | + |
æ
ç
è |
e2
4pe
0 · r | – E |
ö
÷
ø |
· y(x,y,z) = 0 |
mit r = (x2 + y2 + z2)1/2 |
|
 |
Damit sind wir auf dieser Stufe vielleicht nicht mit unserem Latein, aber doch
mit unserer Mathematik am Ende, denn diese Gleichung können wir nicht so schnell lösen wie das für den Fortgang
der Vorlesung nötig wäre. Für die mathematisch Interessierten ist der Lösungsweg aber im Link: Schrödingergleichung und Wasserstoffatom beschrieben. |
 |
Wir können aber einfach akzeptieren
, daß diese Differentialgleichung bekannte Lösungen hat, die wir im folgenden beschreiben. Zunächst
stellen wir fest, daß es (unendlich) viele Lösungen dieser Schrödinger-Gleichung
für das Wasserstoffatom gibt, sie unterscheiden sich in mindestens einer von drei
Quantenzahlen, die fester Bestandteil der Lösung sind. Diese drei Quantenzahlen
haben Namen: |
|
 |
Hauptquantenzahl
n = 1, 2, 3,
..., d.h. alle positiven natürlichen Zahlen beginnend mit 1. |
|
 |
Nebenquantenzahl
l = 0, 1, 2,
3, ..., (n – 1), d.h. alle natürliche Zahlen sind erlaubt, die um 1 kleiner sind als n
. |
|
 |
magnetische Quantenzahl
m
= l, l – 1, ..0,.., - l, d.h. alle ganzen Zahlen zwischen – l and +
l sind erlaubt. |
 |
Dazu kommt noch eine vierte Quantenzahl, die
zwar nicht aus der Schrödingergleichung "herauskommt", aber als eine Grundeigenschaft des Elektrons sich
(trivial) überlagert, die: |
|
 |
Spinquantenzahl
s = +1/2 oder
– 1/2 - unabhängig von allen anderen Quantenzahlen |
 |
s, wie gesagt, ist dabei nicht eine aus der Lösung der Schrödingergleichung
abfallende Quantenzahl, sondern kommt von der fundamentalen Eigenschaft des Elektrons, wie auch aller anderen Elementarteilchen, einen Spin zu haben - wir werden das in Kürze näher betrachten. |
|
 |
Jede der obigen Lösungen gilt für jede der beiden möglichen Spinquantenzahlen
s - damit verdoppelt sich schlicht die Lösungsmannigfaltigkeit. Um zwischen den beiden Spinquantenzahlen
zu unterscheiden malt man gerne ein Pfeilchen "rauf" oder "runter" sobald man in bildliche Darstellungen
geht. |
|
 |
Für Puristen sei angedeutet: Nimmt man statt der hier dargestellten Schrödingergleichung
die oben schon erwähnte erweiterte Form der Dirac Gleichung, ist auch der Spin
in der Grundgleichung enthalten. |
 |
Ein konkreter Satz Quantenzahlen beschreibt damit einen der möglichen Zustände
des Systems. Weiterhin ergibt sich für jede der durch einen Satz Quantenzahlen definierten möglichen Lösungen
oder, einfacher gesagt, für jeden Zustand, eine bestimmte Gesamtenergie
E. Damit erhalten wir das Lösungsschema: |
|
|
| Lösungen: | |
y = yn, l, m, s(x,y,z) |
| | | |
| Zugehörige Energien: | |
E = En, l, m, s |
|
|
© H. Föll (MaWi 1 Skript)