|
Ideale Dielektrika sind perfekte Isolatoren
charakterisiert durch ihre DK er oder durch die Suszeptibilität c. | |
Sinnvolles
Materialgesetz |
| Sinnvolle neue
Materialkonstante |
| Alte
Materialkonstante |
| Beziehung
D Û P
|
|
|
|
 |
Die DK oder die Suszeptibilität eines Dielektrikums folgt aus seiner
Polarisation. | |
|
 |
Die Beziehung zwischen Feld E
und Polarisation P ist aus Materialsicht sinnvoller als die Beziehung zwischen Feld und Verschiebungsdichte. |
|
|
 |
Umrechnungen sind einfach Þ |
|
| |
| |
| |
 |
Reale Dielektrika haben eine endliche Leifähigkeit. |
|
 |
| j(w) | = |
w · e'' · E( w)
| + |
i · w · e' · E(w) |
|
|
|
 |
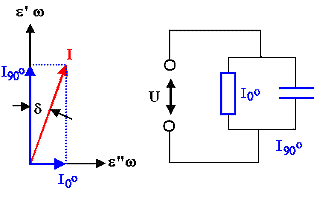
Das läßt sich am einfachsten wie gezeigt beschreiben. Der insgesamt fließende
Wechselstrom wird durch eine komplexe dielektrische Funktion e(w)
erfaßt Þ | |
|
 |
Der Realteil von e' beschreibt den um 90o
phasenverschobenen Teil der Stromdichte j( w); der Imaginärteil e''
den Teil der in Phase fließt. | |
|
 |
Damit sind Wirk- und Blindleistung proportional zu e''
bzw. e'. | |
|
 |
Dies gilt unabhängig davon von welchem Effekt der Imaginärteil resultiert. |
|
|
| |
| |
 |
Ein externes elektrisches Feld wird in einem Dielektrikum immer
Dipole induzieren und
zusätzlich die eventuell vorhandenen Dipole verändern. |
|
|
|
 |
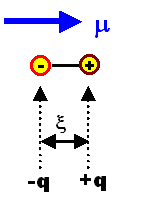
Die Polarisation eines Dielektrikum ist die Vektorsumme der enthaltene Dipolmomente per Volumen |
|
 |
Ein Dipolmoment ist definiert wie gezeigt Þ |
|
| |
| |
|
 |
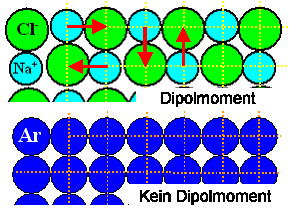
Viele Materialien enthalten Dipomomente (z. B. Ionenkristalle Oxide, Wasser, ...)
andere (Edelgas, dielektrische Elementkristalle) sind neutral. |
|
|
|
 |
Im ersten Fall addieren sich die vorhandenen Momente ohne Feld i.d.R. zu P
= 0 C/cm2 ; mit Feld wird die Ausrichtung so geändert, dass P
¹ 0 C/cm2 resultiert. |
|
| |
| |
| |
 |
Es gibt neben der mathematisch schwer greifbaren Grenzflächenpolarisation
drei wesentliche Polarisationsmechanismen. | |
- Atom- oder Elektronenpolarisation
- Ionenpolarisation
- Orientierungspolarisation
|
|
|
 |
Im 1. Fall wird die durch das Feld die Elektronenhülle relativ zum
Atomkern verschoben und dadurch ein Dipolmoment induziert.
- Sehr schwacher Effekt bei kugelförmigen Atomen (Beispiel Edelgase; auch als Kristall; er
= 1,00...)
- Starker Effekt bei gerichteten kovalenten Bindungen (Beispiel typische Halbleiter Si, Ge, GaAs,
...; e r = 15 - 20).
|
|
|
 |
Die Ionenpolarisation ist in allen Ionenkristallen und polaren Bindunge (Oxide, Keramiken)
vorhanden. Mittel bis sehr stark. | |
|
 |
Orientierungspolarisation kommt nur bei Flüßigkeiten vor, da die (Molekül)dipole
sich drehen können müssen. Recht stark; er(H2O) = 80. |
|
| |
| |
| |
 |
In allen Fällen ist die Polarisation proportional zum Feld. |
|
|
|
 |
Damit ist die Grundgleichung "bewiesen"; die Suszeptibität c
kann berechnet werden. | |
© H. Föll (MaWi für ET&IT - Script)