|
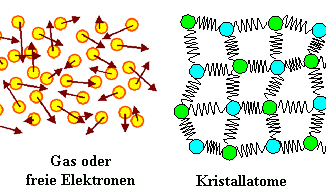
Ein thermodynamisches System besteht aus einer großen Zahl von Teilchen,
die miteinander in Wechselbeziehung in Form von Energieaustausch stehen. |
|
|
|
 |
Es gibt eine definierte Zahl an Möglichkeiten (= Freiheitgrade
f) bei den Teilchen, Energie zu "haben" (Translationsbewegung, Rotation, Schwingung, Potential,
...) | |
|
 |
Im Gleichgewicht gilt dann für klassische
Teilchen der Gleichverteilungssatz (= Definition der Temperatur). |
|
|
| |
|
|
|
| UFreiheitsgrad | = |
½kBT | | |
| |
| UTeilchen | = |
½fkBT |
|
| |
|
| |
| |
 |
Für T
® 0 K folgt UTeilchen = 0 eV; d. h. alle Teilchen
im selbem Zustand Þ |
|
Der Gleichverteilungssatz gilt
nicht
für Fermionen |
|
|
 |
Trotzdem ist im Gleichgewicht die Besetzung der vorhandenen Energie-Zustände
immer dieselbe. | |
| |
| |
|
 |
Es gilt immer der Energieerhaltungssatz = 1.
Haupsatz der Themodynamik . |
|
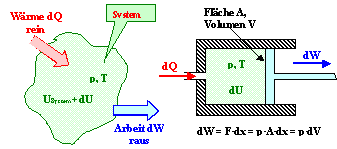 |
| DU = Q
– W |
|
|
 |
Der Gleichverteilungssatz folgt nicht
aus dem 1. Haupsatz. | |
|
 |
Der 1. Hauptsatz regelt nicht, was mikroskopisch vorliegt, d.h. welche innere Energien
U die Teilchen im Mittel haben = welche Energieniveaus durch wieviel Teilchen besetzt sind. |
|
|
 |
Es wird ein 2. Prinzip benötigt. |
|
|
| |
| |
 |
Die Entropie
S ist ein quantitatives Maß für Unordnung. |
|
|
|
 |
Die Zahl pi beschreibt die Zahl der mikroskopisch möglichen
Anodnungen der Teilchen zum selben Makrozustand i . |
|
|
|
| 2. Hauptsatz: |
Im thermodynamischen Gleichgewicht hat ein System eine möglichst große Entropie
und
Die Entropie eines abgeschlossenen Systems wird nie von alleine kleiner |
| |
| Entropie von n Leerstellen und N – n Atomen |
| Sn | = |
kB · ln | æ
è |
| N!
n! · (N – n)! | |
ö
ø | | |
| | |
| | |
= | kB· |
æ
è |
ln N! – ln n! – ln (N – n)! |
ö
ø |
|
|
| |
|
|
| |
|
|
 |
Beispiel: Leerstellen machen Unordnung. Die zugehörige Entropie kann man (mühsam)
ausrechnen. | |
|
| |
| |
 |
Alle Systeme folgen einem einfachen Minimierungsprinzip: |
|
Ein System ist im (thermodynamischen) Gleichgewicht,
sobald die freie
Energie G
minimal ist. |
|
|
Ungeheuer wichtig!
|
|
|
 |
In Worten.
- Mache die innere Energie U so klein als möglich.
- Ziehe davon möglichst viel mit der Temperatur T gewichtete Unordnung = Entropie S
ab.
- Minmiere die erhaltene Zustandsfunktion
G = U – TS.
|
|
|
 |
Es mag sich daher lohnen, bei hohen Temperaturen etwas in innere Energie U zu "investieren"
(z. B. duch Aufbringen der Bildungsenergie von Leerstellen , falls man damit kräftig Entropie bekommt. |
|
|
 |
Grundsätzlich sind damit Systeme bei höheren Temperaturen unordentlicher als bei
niedrigen Temperaturen: Festkörper schmelzen! | |
| |
| |
|
 |
Beispiel Leerstellen: |
|
Freie Energie von
n Leerstellen im Kristall
aus N – n Atomen |
| G(n) | = | E
0 + n · EF – kB
T · ln ( |
N!
n! · (N – n)! |
) |
|
|
|
 |
Aus G = Minimum folgt dG/dn = 0, daraus |
|
|
| |
|
|
|
| |
|
| |
|
|
 |
Läßt sich auf jede atomare Fehlstelle verallgemeinern.
Þ Kristalle wollen bei hohen Temperaturen verdrecken! |
|
|
| |
| |
 |
Alle Systeme sind durch eine Zustandsdichte
D(E) gekennzeichnet: | |
| D(E) = |
dN
dE | = |
Differentielle Zahl dN der
Zustände im Energieintervall
(E, E + dE)
pro cm3 |
|
|
|
 |
D(E) wäre für ein diskretes Energieniveau der
Entartungsgrad. | |
|
 |
Die Zustandsdichte ist eine "doppelte" Dichte: 1. bezüglich der Energie
und 2. bezüglich des Volumens (trivial). | |
|
 |
[D] = eV–1 · cm–3 |
|
|
| |
| |
 |
Bei gegebener Zustandsdichte entscheidet nur
die Besetzung der daduch gebenen Energieniveaus darüber, was das System "tut". |
|
Wie groß ist die Wahrscheinlichkeit dafür, dass ein Platz bei der Energie E besetzt
ist?
(für gegebene Parameter wie Temperatur T, Teilchengesamtzahl N0,
...) |
|
|
 |
Zum Gleichgewicht, d.h. dem Minimum der freien Energie G = U –
TS, gehört eine bestimmte Besetzungssystematik. |
|
|
 |
Die Grund- und Schlüsselfrage ist: Þ |
|
|
| |
| |
 |
Die Antwort auf diese Frage ist eine Verteilungsfunktion
. | |
Bose-Einstein-Verteilungsfunktion (für Bosonen):
Es können beliebig viele Teilchen = Bosonen auf einem Platz sitzen
(z.B. alle bei E = 0
eV bei T=0 K)
Fermi-Dirac-Verteilungsfunktion für Fermionen (= Elektronen):
Es können maximal 2 Elektronen = Fermionen (Spin rauf und runter) auf einem Platz sitzen
(z.B. nicht alle bei E = 0 eV bei T = 0
K) |
|
|
 |
Es gibt genau zwei Verteilungsfunktionen w(E),
| |
|
 |
eine für Bosonen und ein für Fermionen
. | |
| |
| |
| |
 |
Damit ergibt sich als Haupt- und Grundformel für die Konzentration n(E)
an Teilchen bei der Energie E Þ |
|
| n (E ) | = |
Dichte der Plätze mal
Wahrscheinlichkeit der Besetzung mal
Energieintervall |
| = |
D(E) · w(E) · DE
|
|
|
| | |
| |
|
 |
Uns interessiert nur die Fermi-Verteilung; wir nennen sie immer f(E;
EF, T): | |
f(E; EF , T) =
|
1
| | exp
| æ
è |
E – EF
kBT |
ö
ø |
+ 1 |
|
|
|
 |
Wir habe eine Funktion der Energie E mit der Temperatur T und
der Fermienergie EF als Parametern. |
|
|
 |
Die Fermienergie ist eine Systemgröße. Sie ist diejenige Energie, bei der die Wahrscheinlichkeit
einer Besetzung = ½ ist. (Bei T = 0 K und einer kontinuierlichen Zustandsdichte
entspricht das der Energie, bei der das letzte Elektron untergebracht werden kann.) |
|
| |
| |
|
| |
|
| | |
| | |
| |
|
 |
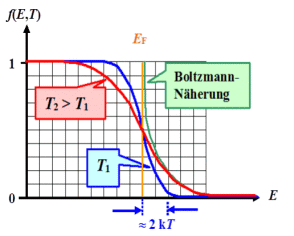
Der Graph der Fermiverteilung sieht - leicht erratbar - so aus Þ |
|
|
 |
Die folgenden Eigenschaften machen das Arbeiten mit der Fermiverteilung einfach: |
|
|
 |
Die "Aufweichungszone" ist » 4 kBT
breit. | |
|
 |
Für den "Hochenergieschwanz", d. h. für Energien einige kBT
oberhalb der Fermienergie, kann die Boltzmann-Näherung verwendet werden: |
|
|
| |
|
|
|
| f(E,T) » exp |
( – |
E – EF
kBT | ) |
|
| |
|
| |
|
|
 |
Die Boltzmann-Näherung bedeutet immer: Die Teilchen können jetzt "klassisch" beschrieben werden. |
|
|
| |
| |
 |
Die Quintessenz des Ganzen ist: |
| |
| |
| |
|
Die Verteilung von Teilchen auf die verfügbaren
Energieplätzen mit der
Fermiverteilung
oder, in klassischer Näherung,
mit der Boltzmannverteilung , beschreibt immer
den Zustand kleinster freier Energie und damit
thermodynamisches Gleichgewicht
(bei einer gegebenen Temperatur T).
|
|
| | |
| |
© H. Föll (MaWi für ET&IT - Script)