|
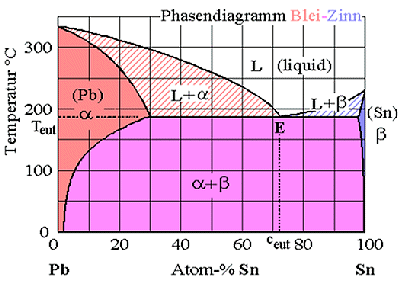
Ein Phasendiagramm gibt für jeden Punkt im Temperatur - Zusammensetzungsdiagramm
an, welche Phase oder Phasen im Gleichgewicht vorliegen |
|
|
|
 |
Zwischen der Zahl der Komponenten C (hier Pb und Sn), die Zahl
der Phasen P die vorliegen, und der Zahl F der Freiheitsgrade (hier Temperatur und Komposition)
die möglich sind besteht eine fundamentale Beziehung, die Gibbsche Phasenregel |
|
|
| |
|
|
|
| |
|
| |
|
|
 |
Für ein binäres Phasendiagramm (d.h. C=2)
und zwei Freiheitsgrade f=2 gibt es dann nur eine
mögliche Phase. | |
| | |
| |
|
 |
Zwei-Phasen Gebiete oder Mischphasen
im Phasendiagramm bestehen deshalb immer aus Phasen fester Komposition: a + b,
L + a, oder L + b). |
|
|
|
 |
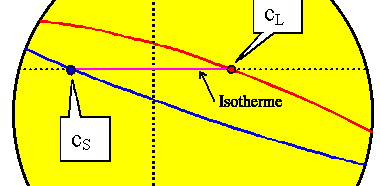
Die beiden Kompositionen ergeben sich aus den Schnittpunkten der Isothermemit
den das Mischphasengebiet begrenzenden Linien. | |
|
 |
Der jeweilige Anteil fa und fb der beiden Phasen ergibt sich aus dem Hebelgesetz |
|
|
| |
|
|
|
| |
|
| |
| |
 |
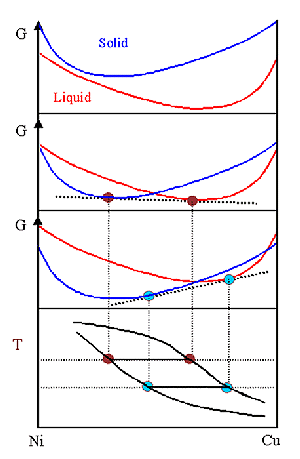
Phasendiagramme erhält man durch Vergleich der freien Enthalpien möglicher
konkurrierende Phasen. | |
|
|
 |
Qualitativ relativ einfach, quantitativ aber schwer. |
|
|
 |
Unmittelbare Konsequenz: Es gibt keine einfachen Phasendiagramme - Mischphasen sind häufig. |
|
 |
Bei Eutektika gibt es einen Punkt (T,
C, d.h. f=0), in dem drei Phasen (L=flüssig + feste a
und b) im Gleichgewicht stehen |
|
|
 |
Im obersten Bild gibt der Punkt "E" die eutektische Komposition, die waagrechte
Linie die eutektische Temperatur. | |
|
 |
Die zugehörige invariante Reaktion (invariant=keineFreiheitsgrade)
lautet | |
|
| |
|
|
|
| |
|
| |
|
|
 |
Weiter invariante Reaktionen führen zu peritektischen, eutektoiden und peritektoiden
Typen von Phasendiagrammen. | |
| | |
| |
 |
Bei gegebener Komposition und Phasendiagramm lassen sich weitreichende Schlüsse
auf das zu erwartende Gefüge ziehen. |
|
|
|
 |
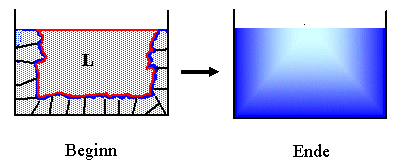
Insbesondere wird unmittelbar klar, daß eine homogene einphasige Schmelze nach dem Erstarren
i.a. keine homogene Zusammensetzung mehr haben wird. | |
|
 |
Ausnahme: Invariante Reaktion, d.h. eutektische Komposition. |
|
 |
Bei vermeintlich einfachen Techniken wie Gießen, Schweißen oder Kristallziehen,
laufen in Wahrheit komplexe Vorgänge ab. | |
|
 |
Die unmittlbare Anwendungen dieser Verfahren ist oft nicht möglich oder bedarf erheblicher
"Tricks". | |
| | |
|
| | |
| |
|
© H. Föll (MaWi 1 Skript)