|
Wir mischen mal 33 % Mo und 67 % Ni (nach Gewicht), schmelzen das
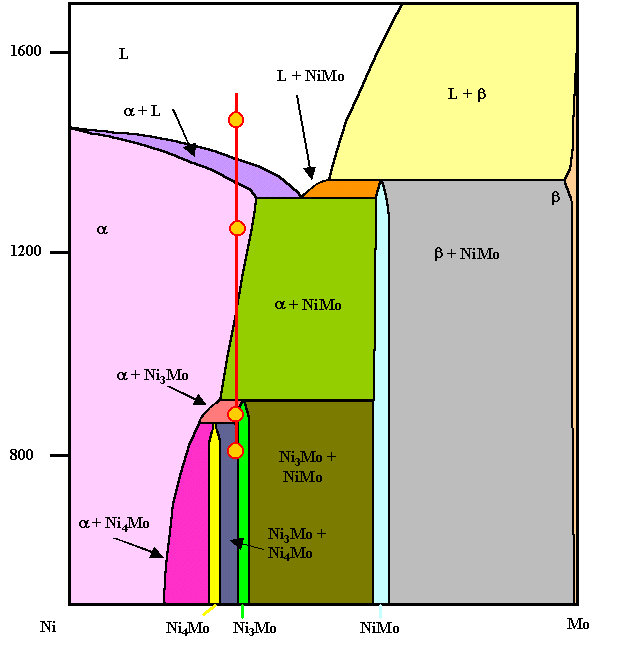
Ganze, und kühlen dann ab. Wir laufen dann entlang der roten Linie im Phasendiagramm in der Temperatur nach unten |
|
 |
Im flüssigen Zustand sind wir dann z.B. am obersten Punkt im
Phasendiagramm - alles ist "L" |
|
 |
Mit beginnende Abkühlung unterschreiten wir bei ca. 1390 oC die Liquiduslinie
und haben jetzt einen zweiphasigen Zustand mit Ni-reichem Feststoff in Mo-reicher
Schmelze. |
|
 |
Beim zweiten Punkt ist alles fest, wir haben eine Phase;
die a-Phase: Ni mit 33 % gelöstem Mo. |
 |
Bei ca. 1070 oC geschieht etwas Neues: Wir passieren die Grenze
zu einem Zweiphasengebiet bestehend aus der stöchiometrischen Verbindung NiMo
und der a-Phase. |
|
 |
Und noch zweimal müssen wir neue Phasengemische produzieren: Beim dritten Punkt haben
wir a + Ni3Mo und beim vierten Punkt schließlich
den Endzustand: Ein zweiphasiges Gemisch aus Ni4Mo und Ni4Mo. |
 |
Ganz schön kompliziert, aber mit der "Landkarte" Phasendiagramm
leicht zu konstruieren. |
 |
Was geht nun eigentlich im Festkörper vor sich, der ja bis zur kompletten
Erstarrung viermal sein Gefüge ändern muß? Auch das schauen wir uns
schematisch an: |
| |
|
© H. Föll (MaWi 1 Skript)