|
Ein Teilchen, oder auch ein ganzes System von Teilchen, befindet sich im Gleichgewicht, falls sich "nichts" mehr ändert. |
|
|
|
 |
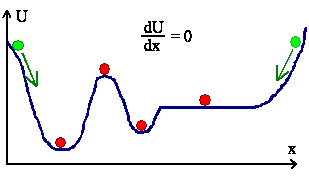
Bei einem klassischen "System" aus nur einem Teilchen ("Massenpunkt")
herrscht Gleichgewicht, falls sich das Teilchen im Minimum der potentiellen Energie befindet und jede Bewegung durch Reibung
beendet ist. | |
|
 |
"Treibende Kraft" in Richtung Gleichgewicht
ist dabei die Minimierung der Energie. | |
| | |
| |
 |
Systeme vieler miteinander wechselwirkender
mikroskopischer Teilchen müssen durch geeignete makroskopische (meßbare) Größen oder Zustandsvariablen
beschrieben werden, die das System hinreichend charakterisieren. | |
Zustandsvariable sind beispielsweise:
- Temperatur
- Druck
- Teilchenzahl
|
|
|
 |
Im umfassenden thermodynamischen Gleichgewicht ändern
sich diese Zustandsvariablen nicht mehr. |
|
|
 |
Treibende Kraft in Richtung Gleichgewicht ist nicht nur die Minimierung der Energie, sondern
auch die Maximierung von "Unordnung". | |
| | |
| |
 |
Thermisches Gleichgewicht bedingt dieselbe
Temperatur T, mechanisches Gleichgewicht denselben Druck p
überall im System. | |
Mechanisches und thermisches
und chemisches Gleichgewicht
= thermodynamisches Gleichgewicht
|
|
 |
Chemisches Gleichgewicht bedeutet, dass sich
die Teilchenzahlen ni nicht mehr ändern. |
|
|
 |
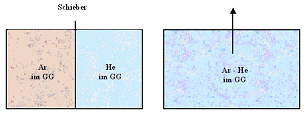
Beispiele:
- Zwei Gase mischen sich bis die (mittlere) Teilchenzahl überall dieselbe ist.
- Salz löst sich in Wasser - bis "Sättigung", d.h. chemisches Gleichgewicht erreicht ist. Die Zahl
der gelösten Ionen ändert sich nicht mehr.
|
|
|
 |
Ein "Teilchen" kann dabei vielerlei sein, z.B. ein Atom, Ion oder Molekül;
aber auch ein Elektron, Photonen, Phonon, Defektelektron (= "Loch"), usw. |
|
 |
Der Begriff chemisches Gleichgewicht ist deshalb
etwas mißdeutig; besser wäre "Teilchenzahlgleichgewicht". |
| |
| | |
| |
 |
Was wir brauchen ist ein thermodynamisches Potential
F = F(Zustandsvariablen) in Analogie zum rein mechanischen Potential. |
|
Gleichgewichtsbedingung für thermodynamisches
Gleichgewicht:
| DF | = |
¶F
¶n1 |
· Dn1 + |
¶F
¶n2 |
· Dn2 + |
¶F
¶n2 |
· Dn3 + ..... |
= 0 |
|
|
|
 |
Thermodynamisches Gleichgewicht liegt dann vor, falls F ein Minimum hat |
|
|
| |
| |
 |
Das Gleichgewicht in einem Systeme vieler Teilchen ist ein dynamisches
Gleichgewicht. | |
|
|
 |
Nur makroskopisch ändert sich nichts, mikroskopisch
kann es trotzdem große Änderungen geben, die sich aber (im Mittel) exakt kompensieren. |
|
|
 |
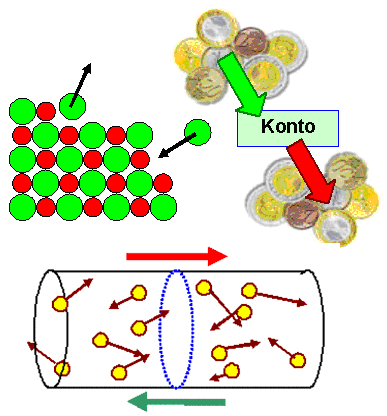
Beispiele: - Salzauflösung: Zahl der Na+
Ionen die in Lösung gehen = Zahl der Na+ Ionen, die sich am Kristall binden.
- Girokonto: Abhebungen = Einzahlungen.
- Strom: Elektronenfluß nach rechts = Elektronenfluß nach links.
|
|
| |
|
|
| | |
|
© H. Föll (MaWi 1 Skript)